时间起始于2026年5月1日零时,国家药监局第38号公告开始生效,此举措使得作为开始的数据呈现出这样的情况,即干细胞药物IND申报周期从原本平均的18个月被压缩到了9个月,并且合规路径第一次出现了所谓的“快车道”。
📍 过去:堵在“细胞质量”这道闸
还记得去年吗?
> 你花三个月修完CMC数据,审评回来又是一轮补正。
> “为什么同样的工艺,别人批了我还在等?”
业内谁没熬过这种追问?
那个时候,《干细胞临床研究管理办法》处于“试行”阶段,每一条细则,都如同悬挂于半空之中的靴子。
📍 现在:2026.5.1划了三条实线
备案制转阶梯式许可
早期探索(Ⅰ期)→ 地方卫健委备案
确证性试验(Ⅱ/Ⅲ期)→ 国家局统一审批
豁免部分“重复性非临床”
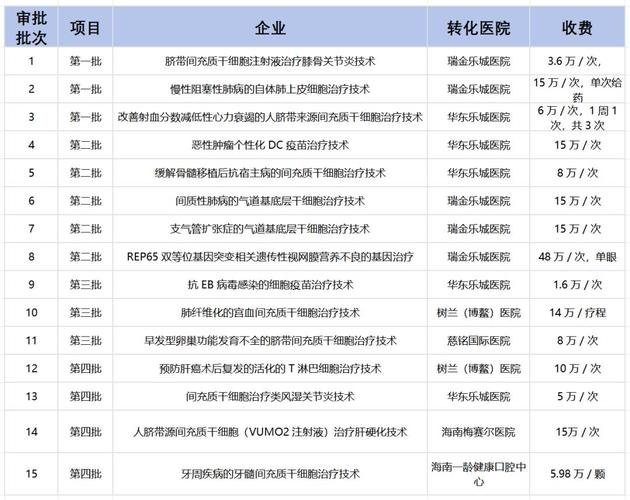
若存在已经有同类产品获得批准的靶点,像脐带间充质干细胞治疗膝骨关节炎这样的情况,新的申报是能够引用公开的毒理数据的。
医院与企业的“双负责人制”
不再单单看申办方,而是PI的签字权重被提升到40%,你来猜猜究竟有多少医院在连夜更改SOP呢?
📍 未来90天:三个动作帮你避坑
把在库的项目找出来,去跟“适应症优先清单”进行对照,这个清单是5月1日附件里所包含的那8个病种对应的清单。
🔹 对质量放行标准予以重新去进行评估,新政有着这样的要求,每一批次都需要额外增加检测“端粒酶活性动态谱”。
和合作的医院重新签订《责任协议》,将“副反应兜底条款”这个内容详细划分到细胞传代的次数方面。
反问一句:
要是在半年之前,你便能够预先判断出这一回的转向,那么目前的管线情形之下,会不会少经过三段呈现出弯曲状态的路线呢?
政策向来都不是那种会阻碍前行的路障物件,而是能够指引方向的路标指示物。5.1出台的新政所去除掉的是那些模糊不清的存在状况,所留存下来的则是能够促使其落地的加快发展速度。
你的项目现在踩在哪一档?

