当我站在2026年春天的起始处回头看时,每一个单一形式存在着的生命个体,都如同是一部尚未完成的有着宏大叙事风格与历史感的诗作。干细胞研究过程当中的每一次向前推进的情形,就仿佛是在这部诗作之上雕刻下全新的可供解释说明的文字注释。有相当数量的人对于国家到底颁布了哪一些相关政策,可能依旧感觉似处于浓厚的迷雾之中而看不清楚。然而答案实际上就隐匿于最近三年里密集进行发布的文件所展现出的脉络里面。
首先,存在着监管框架的一种“系统性重塑”情况。2024年时,《细胞治疗产品生产质量管理规范》出现了升级现象。到了2025年,《人源干细胞产品药学研究与评价技术指导原则》实现了落地。国家不再采取那种“一刀切”式的禁止或者放任的做法,而是构建起一条涵盖从“实验室培养皿”直到“医院手术台”的全链条监管闭环。你会发觉,往昔那种呈现“作坊式”状况的干细胞治疗中心正飞速消逝,这乃是源于政策清晰明确地作出要求,即所有临床级别的干细胞都得在契合药品GMP标准的环境里予以制备。这究竟意味着什么呢?意味着在安全性方面迈入了新的层级,也意味着行业所设置的门槛出现了急剧的提升。
其次,出现了临床应用路径的“双轨制突破”的情况。这儿的一方面是,国家卫健委针对37种难治性疾病,像重症狼疮、脊髓损伤这类,把它们纳入到了干细胞临床研究备案范围之中,还实行了“机构伦理审查+国家备案”这样的快速通道。而另一方面是,国家药监局专为干细胞药物开创了“突破性治疗药物”程序,符合条件的产品其审评时间缩短了40%。这恰似给干细胞疗法构筑了两座桥梁,一座朝着严谨的临床研究而去,另一座径直指向药品的最终上市,你会感到好奇,普通人什么时候能够使用?答案依赖于你是投身于研究性治疗之中,还是等候获批的药物。
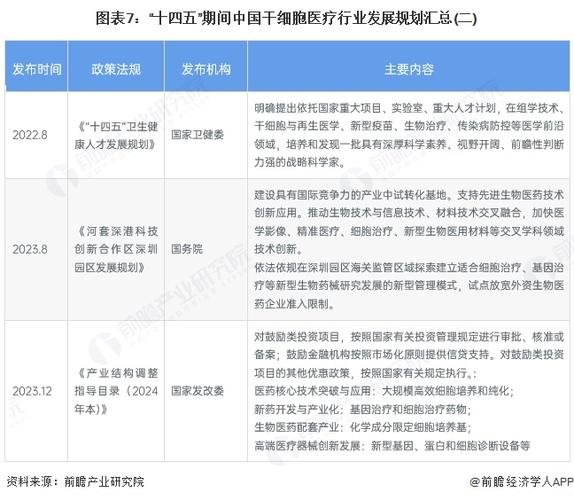
再者,存在伦理与资本的双重“导向阀”,2025年底颁布了《细胞治疗伦理审查指南》,该指南首次把“患者知情同意权”细化成12项必须逐条确认的清单,并严厉打击“干细胞旅游”等地下交易,在资本端,发改委把“细胞治疗药物研发和生产”列入《产业结构调整指导目录》的鼓励类,给予税收减免和专项补贴。一边是伦理方面犹如坚固铁闸般的存在,一边是资本领域好似源源不断活水一样的情形,这样一种看上去存在矛盾的组合,恰恰预示着所在行业正处在从以往那种野蛮生长状态逐渐步入到理性繁荣阶段的转折点上。
最为关键的要点,也是极具往后现代感的,乃是区域范畴之内进行试点的“政策特区”。海南那个名为博鳌乐城的地方、上海的张江地区、深圳的前海区域等,这五个不同的地区,被授予了“先行一步去尝试”这样的特殊权利,准许进口外面其他些国家已经在市场上售卖了的、然而在咱们国内却还没有得到批准许可的干细胞相关产品,并且着手开展基于真实世界状况的数据探索研究。试着去设想一下呀,当个中的一位患上少见遗传病的患者,根本不需要长途跋涉,漂洋过海到别的地方去,在海南这个地方就能够使用上于欧洲获得了批准认可的干细胞类药物——这可不仅仅只是体现出政策原本所具备的那种温暖之感,更是咱们中国以一种姿态,融入到全球整个再生医学所涌起的那股浪潮当中了呢。
处于季节的转角之处,春风当中裹挟着变革所带来的凉意,从混沌状态朝向有序状态,从封闭情形变为开放情形,国家针对干细胞政策的每一回调整,皆是在寻觅那个最为微妙的平衡点,那就是既不让创新的火种因过度管制而熄灭,又不让逐利的狂潮将安全的堤坝冲垮,政策向来不是束缚因素,而是一幅无声的航海图,当我们切实读懂这些条款之间的呼吸以及脉动之时,便也读懂了在这个时代背景下,科学怎样敬畏生命,同时治理如何托举未来。

